Влияние олигосахаридов хитозана на выносливость при физических нагрузках
Хитоолигосахарид стимулирует митохондриальный биогенез и повышает выносливость при физической нагрузке посредством активации Sirt1 и AMPK у крыс.
PLoS One. 2012; 7(7): e40073.
Published online 2012 Jul 11. doi: 10.1371/journal.pone.0040073
Авторы: Hyun Woo Jeong, Si Young Cho, Shinae Kim, Eui Seok Shin, Jae Man Kim, Min Jeong Song, Pil Joon Park, Jong Hee Sohn, Hyon Park, Dae-Bang Seo, Wan Gi Kim, Sang-Jun Lee.
Аннотация
Катаболизируя глюкозу и липиды, митохондрии производят АТФ для удовлетворения потребностей организма в энергии. Когда количество митохондрий мало, а их активность низкая, организм человека легко устает из-за недостатка АТФ. Поэтому контроль количества и функций митохондрий важен для оптимизации энергетического баланса. Увеличивая митохондриальную емкость, можно улучшить энергетический обмен и выносливость при физической нагрузке. Путем скрининга различных функциональных пищевых ингредиентов, мы обнаружили, что олигосахарид хитозана (COS) является эффективным индуктором митохондриального биогенеза. У грызунов COS увеличивает содержание митохондрий в скелетных мышцах и повышает выносливость при физической нагрузке. В культивируемых миоцитах, экспрессия основных регуляторов митохондриального биогенеза и ключевых компонентов митохондриальной цепи переноса электронов была повышена при обработке COS. COS-опосредованная индукция митохондриального биогенеза была достигнута частично путем активации молчащего информационного регулятора двух ортологов 1 (Sirt1) и AMP-активированной протеинкиназы (AMPK). Таким образом, можно предположить, что COS может действовать как миметик упражнений, вызывая митохондриальный биогенез и повышая выносливость упражнений посредством активации Sirt1 и AMPK.
Введение
Хитозан, линейный полисахарид, состоящий из глюкозамина, вырабатывается из хитина, который является основным элементом экзоскелета ракообразных, таких как крабы и креветки. Из-за его потенциального положительного воздействия [1] - [5] хитозан широко используется в качестве источника пищи и биомедицинского агента. Олигосахарид хитозана (COS) - смесь глюкозаминового полимера различной длины, является ферментативным продуктом хитозана. COS проявляет ряд благоприятных эффектов: противомикробный / антибактериальный, противораковый, ранозаживляющий эффект [6] - [13]. В [14] ученые предположили, что COS оказывает эффект снижения усталости посредством улучшения митохондриальной функции и усиления митохондриального биогенеза. Тем не менее, основной механизм COS-опосредованного усиления митохондриальной функции остается неясным.
Митохондриальный биогенез представляет собой сложный процесс, включающий координацию ряда белков, происходящих как из митохондриальных, так и ядерных генов. Хотя основной механизм митохондриального биогенеза не совсем понятен, рецептор гамма-коактиватора 1, активируемый пролифератором пероксисом (PGC1), участвует в качестве главного регулятора биогенеза митохондрий посредством взаимодействия с ядерным респираторным фактором 1 (NRF1) [15], [16]. NRF1 инициирует транскрипцию генов, ответственных за конструирование митохондрий, а PGC1α устанавливает сеть регуляции генов для митохондриального биогенеза.
Недавно было высказано предположение, что экспрессия и активность PGC1α регулируются АМФ-активированной протеинкиназой (AMPK) и регулятором информации двух ортологов 1 (Sirt1) [17] - [19]. Оба белка способны чувствовать внутриклеточную энергию и / или состояние питания. Например, AMPK активируется в стрессовых условиях, включая голодание и осмотический шок, для запуска образования АТФ, способствуя утилизации глюкозы и жирных кислот, тем самым облегчая метаболические дисфункции, такие как гипергликемия и гиперлипидемия. [20]. Sirt1, NAD+ - зависимая гистондеацетилаза, также активируется голоданием и ограничением калорий [21], [22]. Как и AMPK, Sirt1 широко ассоциируется с энергетическим обменом [23], [24]. Поскольку AMPK и Sirt1 участвуют в митохондриальной функции [23], [25], [26], активаторы этих ферментов могут усиливать митохондриальный биогенез и выносливость.
В этом исследовании мы продемонстрировали, что COS увеличивает содержание митохондрий в скелетных мышцах и повышает выносливость у крыс. Из-за длительной физической нагрузки у грызунов, получавших COS, наблюдалось снижение уровня триглицеридов и холестерина в крови. В дифференцированных миоцитах C2C12 COS усиливает экспрессию и активность PGC1 - одного из важнейших факторов митохондриального биогенеза. В результате COS увеличил количество митохондрий и экспрессию компонентов цепи переноса электронов (ETC). COS-индуцированная активация PGC1 и митохондриальный биогенез опосредовались активацией AMPK и Sirt1. Основываясь на этих данных, мы предполагаем, что COS является эффективным регулятором метаболизма, который действует частично, вызывая митохондриальный биогенез и повышая выносливость при физической нагрузке посредством активации AMPK, Sirt1 и PGC1.
Результаты
COS увеличивает содержание митохондрий в скелетных мышцах крыс, чтобы продлить выносливость к упражнениям
Перед экспериментами in vitro и in vivo мы провели LC-MS / MS анализы для определения состава COS. Как показано в таблице 1 , COS состоит из смеси полимеров глюкозамина различной длины. Средняя молекулярная масса COS составляет 505,63 дальтон, а основным компонентом COS считается димер.
Таблица 1. Состав COS.

В предыдущем исследовании мы продемонстрировали, что COS способен улучшить функцию митохондрий и улучшить устойчивость к усталости [14]. Чтобы быть уверенным, что COS-опосредованное улучшение митохондриальной функции сопровождает повышенное содержание митохондрий и повышенную выносливость к нагрузкам, мы вводили COS крысам. Примечательно, что влажная масса подошвенной мышцы (медленно сокращающаяся мышца, которая содержит большое количество митохондрий) была увеличена после лечения COS без значительных изменений массы тела и потребления пищи (Таблица 2). Уровни аланинаминотрансферазы (ALT) и аспартатаминотрансферазы (AST) в плазме не изменились (таблица 2), что указывает на то, что COS не вызывает токсичности для печени.
Таблица 2. Биологические параметры COS-обработанных крыс.

Одновременно с увеличением мышечной массы подошвы содержание митохондрий также увеличивалось у крыс, которым вводили COS (фиг. 1A). Относительный уровень экспрессии мРНК ключевых генов для митохондриального биогенеза и энергетического метаболизма, таких как PGC1α, NRF1 и карнитин-пальмитоилтрансфераза 1b (CPT1b), был увеличен в скелетных мышцах крыс, которым вводили COS (фиг. S1). В соответствии с повышенным содержанием митохондрий, у животных, которым вводили COS, наблюдалась длительная выносливость к упражнениям (фиг. 1B), независимо от накопления лактата (фиг. 1C), репрезентативного маркера мышечной усталости. Таким образом, возможно, что COS может помочь увеличить содержание митохондрий и повысить выносливость при физической нагрузке.
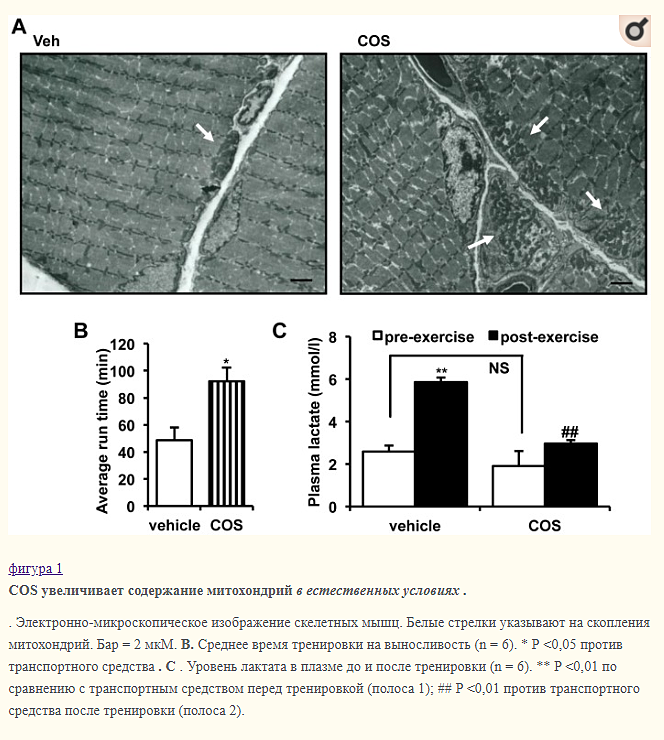
COS индуцирует митохондриальный биогенез
С помощью экспериментов на грызунах мы продемонстрировали, что COS увеличивает митохондриальное содержание в скелетных мышцах и повышает выносливость при физической нагрузке. Затем мы выполнили несколько анализов in vitro для определения основного механизма COS-опосредованного улучшения митохондриальной функции.
Энергетическая эффективность митохондрий зависит как от митохондриальной функции (мембранный потенциал), так и от количества (числа). Чтобы исследовать, способна ли COS индуцировать митохондриальный биогенез, мы измерили плотность митохондрий в дифференцированных миоцитах C2C12 после обработки COS. Подобно результатам in vivo (фиг. 1A), COS также увеличил плотность митохондрий в культивируемых миоцитах (фиг. 2A). Одновременно с повышенной плотностью митохондрий наблюдается экспрессия белка в нескольких компонентах ETC митохондрий, включая подкомплекс 9 NADH-дегидрогеназы 1α (NDFUA9), субъединицу A сукцинатдегидрогеназного комплекса (SDHA), основной белок 2 убихинол-цитохром-с-редуктазы (UQCRC2), субтохромоксидазу (субтохромоксид) COX1) и α-субъединица 1 комплекса АТФ-синтазы митохондрий F1 (ATP5a) активировали в COS-обработанных клетках, обработанных COS ( фиг. 2B и фиг. S9A ).
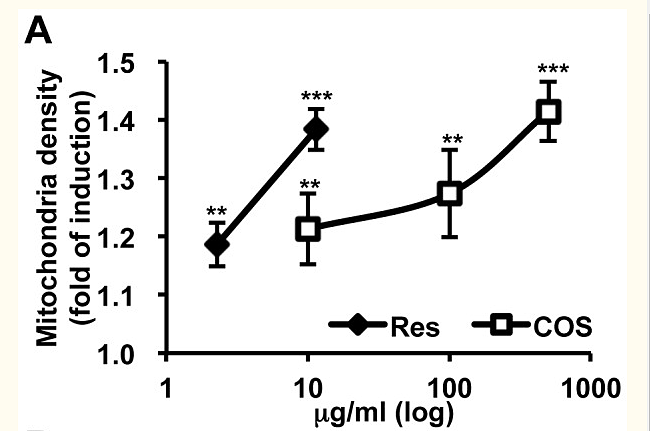
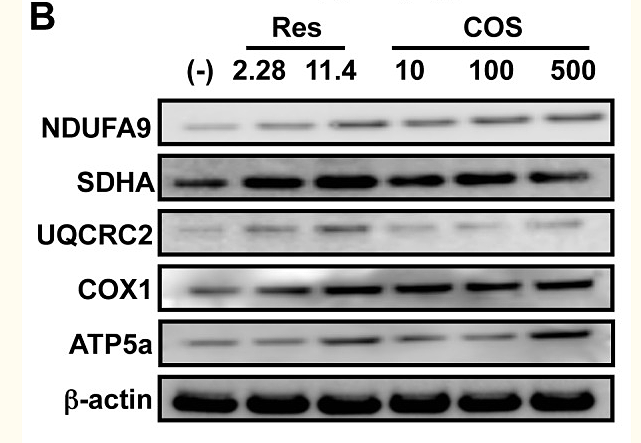
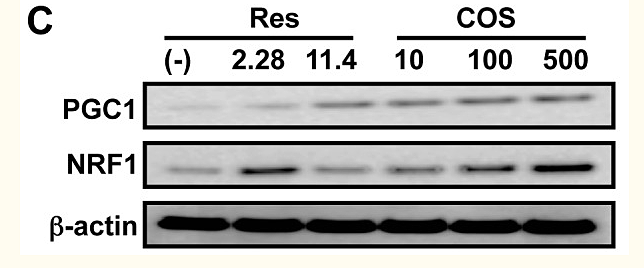

NRF1 и PGC1 являются важными факторами митохондриального биогенеза, индуцируя транскрипцию tfam [15]. Чтобы выяснить, способна ли COS регулировать эти регуляторы транскрипции, мы исследовали экспрессию генов, связанных с митохондриальным биогенезом. Как и ожидалось, экспрессия мРНК PGC1α, PGC1β, NRF1 и tfam была увеличена после обработки COS (фиг. S2). В соответствии с увеличением экспрессии мРНК уровень белка PGC1 и NRF1 также повышался при обработке COS (фиг. 2C и фиг. S9B). Основываясь на этих данных, мы предполагаем, что COS активирует транскрипционный каскад, ответственный за митохондриальный биогенез.
COS активирует Sirt1, PGC1 и AMPK
Сообщается, что Sirt1 активирует PGC1 путем деацетилирования во время митохондриального биогенеза [18] , [19] , [23] , [27] . Чтобы определить, может ли COS индуцировать митохондриальный биогенез путем активации Sirt1, мы измерили активность Sirt1. Как показано на рис. 3А , COS увеличила активность Sirt1.
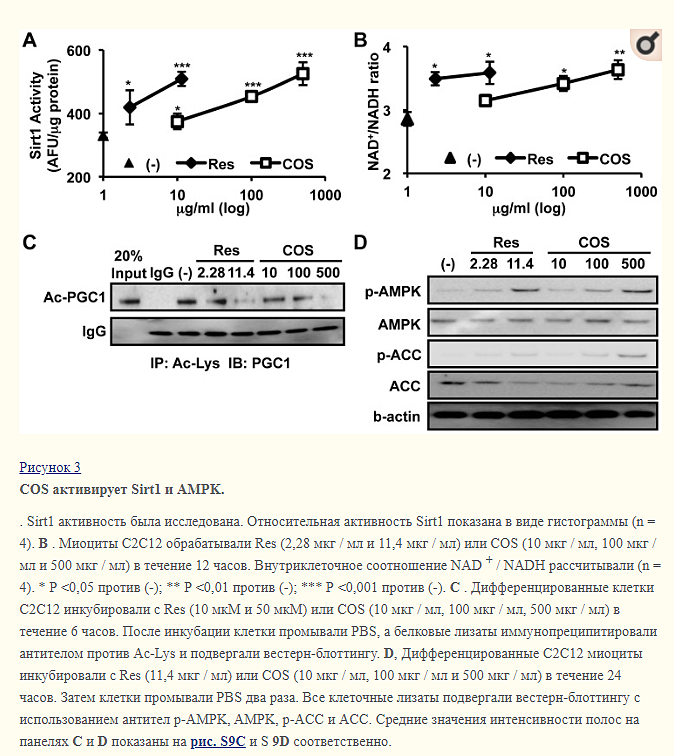
Поскольку Sirt1 требует NAD+ в качестве субстрата, ферментативная активность Sirt1 зависит от клеточного отношения NAD+ / NADH. Чтобы определить, регулирует ли COS внутриклеточное соотношение NAD+ / NADH для активации Sirt1, мы измерили изменения в клеточном соотношении NAD+ / NADH. Как и ожидалось, COS дозозависимо увеличивал клеточное соотношение NAD+ / NADH в клетках C2C12 (фиг. 3B). Эти данные указывают на то, что COS может активировать Sirt1 путем повышения клеточного отношения NAD+ / NADH. В результате уровень ацетилирования PGC1, который отрицательно отражает активность PGC1, снижался при обработке COS (фиг. 3C и фиг. S9C).
Также как и Sirt1, AMPK также стимулирует митохондриальный биогенез и усиливает окисление жирных кислот [20], [25], [28], [29]. Поэтому мы оценили, индуцировала ли COS активацию AMPK. Как и ожидалось, COS увеличил фосфорилирование остатка Thr 172 субъединицы AMPKα с последующим фосфорилированием остатка Ser 79 из ацетил-Со-А-карбоксилазы (ACC) (фиг. 3D и фиг. S9D), субстрата AMPK. Эти данные предполагают, что COS, вероятно, активирует Sirt1 и AMPK, которые ответственны за митохондриальный биогенез.
COS-опосредованный митохондриальный биогенез является Sirt1- и AMPK-зависимым
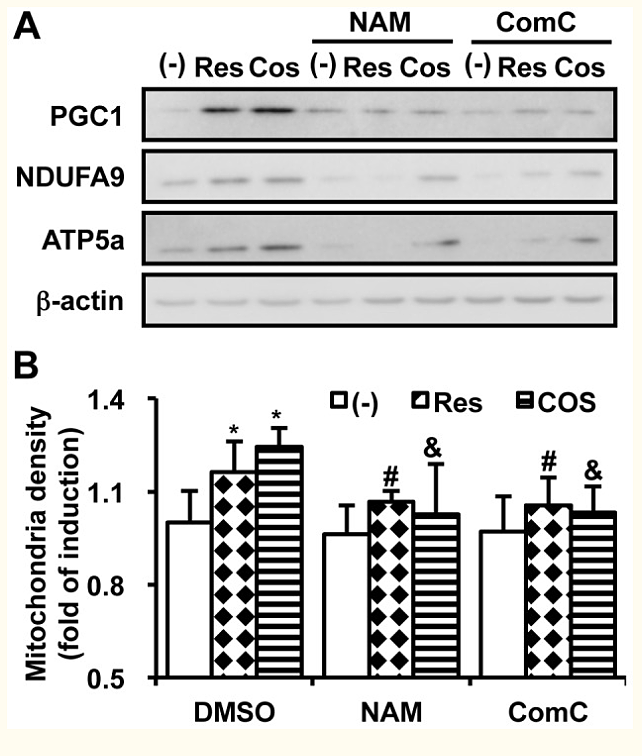
Мы продемонстрировали, что COS активирует Sirt1 и AMPK, две регуляторные молекулы, которые вызывают митохондриальный биогенез. Чтобы определить, опосредуют ли Sirt1 и AMPK влияние COS на митохондриальный биогенез, мы предварительно обработали никотинамид (NAM; ингибитор Sirt1) и соединение C (ComC; ингибитор AMPK). Как и ожидалось, экспрессия мРНК PGC1α, NRF1, PGC1β и tfam была отменена предварительной обработкой NAM или ComC (фиг. S3). Следовательно, COS-опосредованное увеличение уровня белка PGC1 блокировалось предварительной обработкой NAM и ComC (фиг. 4A и фиг. S9E). Индукция NDUFA9 и ATP5a, митохондриальных компонентов ETC, также была предотвращена ингибированием Sirt1 и AMPK (фиг. 4A). После ингибирования Sirt1 или AMPK COS-опосредованный митохондриальный биогенез не наблюдался (фиг. 4B).

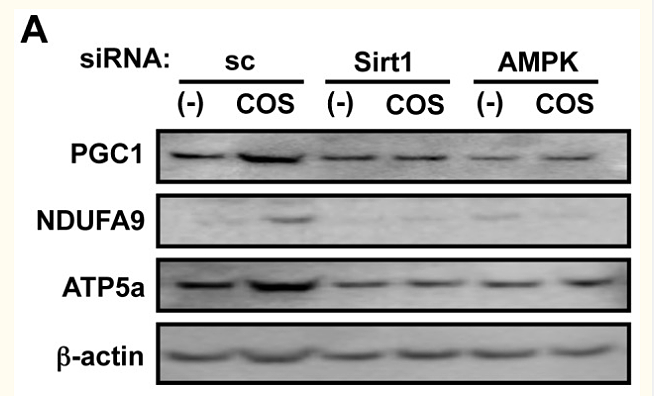
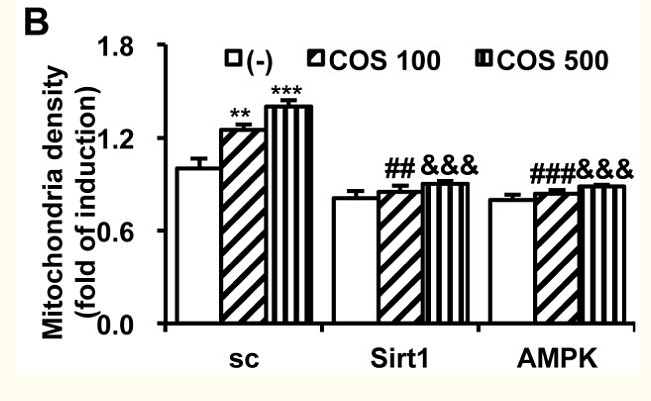
Однако сообщается, что ComC ингибирует активацию HIF-1 независимо от AMPK [30], подразумевая, что ComC может не действовать как специфический ингибитор AMPK. Более того, NAM фактически действует как активатор Sirt1 в низких дозах. Поэтому мы также использовали миРНК для специфического подавления активности Sirt1 и AMPK. Снижение уровня экспрессии Sirt1 и AMPK путем трансфекции siРНК показано на фиг. S4 и S9F . Хотя siRNA скремблирования (sc) не влияла на влияние COS на экспрессию митохондриальных генов (фиг. 5A ) и митохондриальный биогенез (фиг. 5B ), siRNAs, нацеленные на Sirt1 и AMPK, притупляли экспрессию митохондриальных белков ETC (фиг. 5A ) и митохондриальный биогенез (фиг. 5B) после лечения COS, соответственно. Уровни экспрессии митохондриальных белков в клетках, трансфицированных миРНК, показаны на фиг. S9G . В совокупности эти данные указывают на то, что активация Sirt1 и AMPK будет важным шагом в опосредовании влияния COS на митохондриальный биогенез.

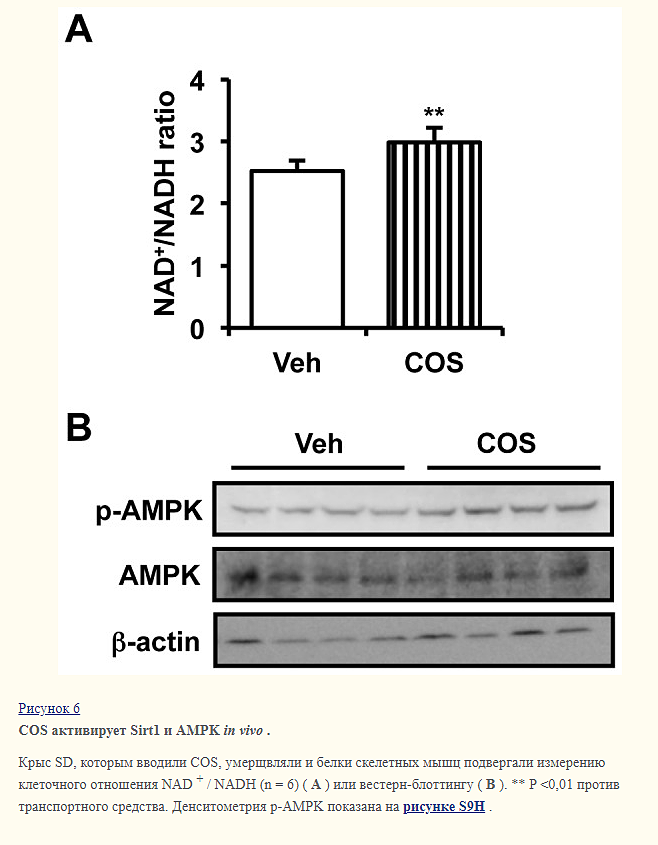
COS активирует Sirt1 и AMPK in vivo
Предполагается, что Sirt1 и AMPK участвуют в сигнальных путях для посредничества в COS-индуцированном митохондриальном биогенезе в культивируемых миоцитах. Чтобы подтвердить, способен ли COS активировать эти белки in vivo , мы исследовали активность Sirt1 и AMPK в скелетных мышцах крыс, которым вводили COS.
Сначала, чтобы определить активность Sirt1, мы измерили соотношение NAD+ / NADH внутримышечно. Подобно экспериментам in vitro (фиг. 3А), COS увеличивает отношение NAD+ / NADH в скелетных мышцах (фиг. 6А), подразумевая, что COS модулирует активность Sirt1 как in vivo, так и in vitro . Затем мы исследовали активность AMPK в скелетных мышцах с помощью вестерн-блоттинга. Как показано на фиг. 6B и S9H , введение COS увеличивало уровень фосфорилирования каталитической субъединицы AMPKα, предполагая, что COS способен активировать как Sirt1, так и AMPK in vivo. Соответственно, наши данные убедительно свидетельствуют о том,COS является новым активатором Sirt1 и AMPK.
Обсуждение
Из-за регулирующей роли в энергетическом балансе митохондрии связаны с различными заболеваниями, включая нарушения обмена веществ, болезнь Альцгеймера, болезнь Паркинсона, рак и старение [31] - [37]. Следовательно, поддержание митохондриальной функции играет существенную роль в поддержании здоровой жизни. Ранее мы продемонстрировали, что COS способен улучшить функцию митохондрий и устойчивость к усталости у мышей [14]. В этом исследовании мы проанализировали состав COS и определили молекулярный механизм COS-опосредованного митохондриального биогенеза. COS инициирует общий процесс митохондриального биогенеза. COS активировал AMPK, Sirt1 и PGC1, чтобы вызвать митохондриальный биогенез в миоцитах. У грызунов COS увеличивает содержание митохондрий в скелетных мышцах и повышает выносливость при физической нагрузке. Интересно, что хитозан (средняя молекулярная масса 9000 Дальтон) не смог имитировать митохондриогенный эффект COS (данные не показаны), что указывает на то, что индукция митохондриального биогенеза является уникальным свойством COS.
PGC1, который активируется во время упражнений, является важным индуктором митохондриального биогенеза и изменения типа мышечных волокон [16], [38] - [40], которые напрямую связаны с энергетическим обменом. Сообщалось, что у пациентов с диабетом 2 типа наблюдалось снижение экспрессии PGC1α и снижение содержания митохондриальной ДНК [41]. PGC1β также участвует в митохондриальном слиянии, которое напрямую связано с функцией митохондрий [38], Эти результаты подчеркивают важную роль PGC1 в поддержании митохондриальной функции и энергетического обмена. Как главный регулятор митохондриального биогенеза, комплекс NRF1 / PGC1 регулирует гены, связанные с митохондриальным биогенезом (например, tfam), а tfam отвечает за индукцию митохондриальных генов [42]. Следовательно, было бы разумно предположить, что PGC1 также способен регулировать экспрессию митохондриальных генов. В настоящем исследовании мы обнаружили новое вещество, способное регулировать как экспрессию, так и активность PGC1. Эти данные предполагают, что COS может быть новым индуктором митохондриального биогенеза и усилителем энергетического метаболизма посредством активации пути PGC1.
Активность PGC1 в основном регулируется Sirt1 и AMPK [17] - [19], [28], [43], которые также регулируют энергетический обмен и митохондриальный биогенез. В наших экспериментах блокада активности Sirt1 и AMPK химическими ингибиторами и специфическими миРНК, которые более специфичны, чем химические ингибиторы (NAM и ComC), аннулировали влияние COS на митохондриальный биогенез. В присутствии этих молекул COS не увеличивал экспрессию митохондриальных компонентов ETC и облегчал митохондриальный биогенез. Хотя основной механизм COS-индуцированной активации Sirt1 и AMPK требует дальнейших исследований, наши данные показывают, что активация Sirt1 и AMPK важна для индукции митохондриального биогенеза при лечении COS.
После увеличения плотности и активности мышечных митохондрий у грызунов мы продемонстрировали, что COS продлевает выносливость при физической нагрузке без избыточного накопления лактата. Более того, ферментативная активность лактатдегидрогеназы (ЛДГ) и креатинкиназы (КК), маркеров мышечного повреждения, не была повышена в группе COS после упражнений на выносливость по сравнению с таковой в группе носителя (фиг. S5), что указывает на то, что COS также повышает клеточную активность, стрессоустойчивость. Наши результаты свидетельствуют о том, что COS замедляет мышечную усталость и повышает выносливость при физической нагрузке, аналогично другим митохондриальным усилителям [44] - [48].
Уровень липидов в плазме тесно связан с метаболическими синдромами, такими как гиперлипидемия и резистентность к инсулину [49], [50]. Сообщалось, что регулярные физические упражнения, которые способствуют утилизации липидов, снижают липидные параметры плазмы и улучшают чувствительность к инсулину [51] - [55]. В наших экспериментах у животных, которым вводили COS, наблюдалось снижение уровня триглицеридов (TG) и холестерина в плазме (фиг. S6). Кроме того, COS увеличивает окисление жирных кислот в культивируемых миотрубках (фиг. S7). Следовательно, вероятно, что крысы, которым вводят COS, могут предпочесть липиды, чем глюкозы, чтобы продлить выносливость при физической нагрузке. Согласно этим данным, было бы разумно, чтобы COS мог быть полезен для облегчения гиперлипидемии и ее пагубных последствий посредством утилизации липидов и наращивания физических нагрузок в скелетных мышцах.
Было бы интересно идентифицировать активное соединение COS. Используя LC-MS / MS анализ, нам удалось проанализировать состав COS и получить несколько низкомолекулярных (LMW) форм COS (от димера до тетрамера). Однако другие компоненты (пентамер или более высокая молекулярная масса) не могли быть разделены, потому что они были элюированы почти в одно и то же время (данные не показаны). Из-за этих технических проблем нам пришлось тестировать только форму COS LMW. Удивительно, но форма COS LMW не вызывала активации Sirt1 (фиг. S8A). Более того, им также не удалось фосфорилировать AMPK и увеличить экспрессию PGC1 и NDUFA9 (фиг. S8B и 9I), гены, которые отвечают за митохондрии. Несмотря на технические ограничения, мы обнаружили, что НМК-форма COS не обладает митохондриогенным эффектом в культивируемых миотрубках. Мы предполагаем, что активный компонент COS может находиться во фракции с высокой молекулярной массой (HMW). И это было бы причиной того, что влияние COS на митохондриальный биогенез было меньше, чем влияние Res в более высокой дозе. Res является чистым химическим веществом, тогда как COS представляет собой смесь активного (HMW) и неактивного (LMW) глюкозамина. Доля HMW, которая, как считается, содержит активное соединение, составляет менее 20% от общего количества COS (таблица 1), тем самым ограничивая активность смеси COS. Дальнейшие исследования с использованием современных методов очистки позволят нам идентифицировать активный компонент COS во фракции HMW и повысить активность COS.
Таким образом, COS активировал AMPK и увеличил клеточное соотношение NAD+ / NADH, чтобы вызвать активацию Sirt1. Активация AMPK и Sirt1 увеличивала экспрессию и активность PGC1 и увеличивала экспрессию митохондриальных генов. В результате активации AMPK, Sirt1 и PGC1, COS способствовал биогенезу митохондрий. У грызунов введение COS значительно увеличивало внутримышечное содержание митохондрий, что приводило к увеличению выносливости при физической нагрузке и уменьшению липидного профиля в плазме. В совокупности наши данные свидетельствуют о том, что COS может повысить выносливость упражнений, способствуя митохондриальному биогенезу.




